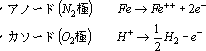|
腐食については、ユーリック著「腐食反応とその制御」で勉強させてもらった。この書籍は腐食に関して最も著名なものである。出版社等については参考文献に記載した。
|
| 5.1 |
はじめに |
|
構造物,機械や圧力容器などにおいて,従来から腐食が問題になっている。これらの問題を解決する意義は
(1).腐食により生ずる物質的な損害を軽減すること。
(2).稼働しつつある装置や機械の安全性の向上である。
(3).金属資源の保存。
(4).外観の美しさを保持する。
などである。(1)の間接的損失、例えば,操業の一時休止,製品の損失,効率の低下,製品の汚染,過剰設計等を考えれば,意義は計りしれない。
|
| 5.2 |
腐食の電気化学的機構 |
|
| (1) |
乾電池との類似性-Faradayの法則 |
|
腐食(Corrosion)は,金属がそれを取り囲む環境によって,化学的あるいは電気化学的に侵食されることを言う。“さびる”という言葉は,とくに鉄あるいは鉄合金が腐食して,主として水化した酸化第二鉄からなる腐食生成物を生成する場合にのみ使い,非金属は腐食するとはいうが“さびる”とは言わない。
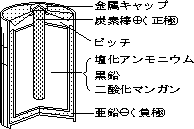
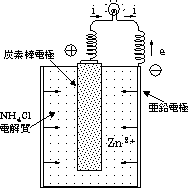
図5.1に示すように,乾電池は中心の炭素棒電極とそれを取り巻く円筒状亜鉛電極とからできており,塩化アンモニウムを主体とする電解質がその間を満たしている。両極上でおこる化学反応によつて電気エネルギー発生し,両極に接続した電球をともす。炭素棒電極(正極)では還元反応がおこり,亜鉛電極(負極)では酸化反応がおこって金属亜鉛が水和した亜鉛イオンZn++・nH2Oに代わる。亜鉛の腐食量は,両極問を流れる電流が大きくなるほど増大するが,Michael Faradayはその定量的な関係を次式で示した。 これを『Faradayの法則』と言う。
金属の反応量(重量,g)=k×電流(A)×時閏(sec)
式の定数kを電気化学当量といい,金属により決まった値である
乾電池を抵抗の小さい金属線て短絡すると亜鉛電極は数時間以内に腐食によって穴があくが,導線を接続しない状態では亜鉛の消耗は極めて少なく,この状態のわずかな亜鉛の消耗は鉄のような不純物により,この不純物は炭素電極と同しような働きをし、電流が亜鉛と不純物の間に流れ亜鉛は腐食する。このような電流を局部電流といい,相当する電池を『局部電池,|ocalaction cell』と言う。 |
|
 |
 |
| 解放時 |
負荷短絡時 |
図5.1 乾電池の原理
|
| (2) |
金属における局部電池の形成 |
|
いかなる金属の表面も,数多くの電極から成り立っていると考えてよい。図5.2のように,その金属体自身を通して電気的に短絡されて,金属が乾燥している間は局部電流は流れないが,水または水溶液中に浸されると局部電池が活動可能になり、それに伴う化学反応によって金属は腐食する。いいかえれば,水,塩類の水溶液,酸,アルカリなどによる金属の腐食は,金属表面を流れる局部電流によるものと言うことができる。金属表面に局部電池を形成する要因は,不純物、異相,表面が接している環境や湿度が場所によって異なる等であるが,次に,これについて述べる。
|
| (a) |
異種電極電池 |
|
この種の代表的なものは乾電池である。電導性の不純物,異種金属の接触,異なる組織の存在による。
・電導性の不純物が異相として接触
・銅管と鉄管の接触
・冷問加工材と焼鈍材の接触
・結晶境界と結晶粒子
・その他 ごみの吸着,表面の凹凸 |
|
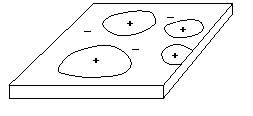
図5.2 組織が異なることにより生ずる局部電池
|
| (b) |
濃淡電池(塩濃淡電池) |
|
同一の金属で作られた二つの電極を,濃度の異なる同種の電解質溶液に別々に浸漬したときに形成される電池である。図5.3で1極を濃厚溶液中に,他極を希薄なNacl溶液に入れたときに,両極を短絡すると希薄な溶液中には極板からCuが溶出し(アノード),他の電極には電解質溶液からCuが析出する(カソード)。すなわち,2極上の反応は,各々の電極が浸されている溶液の濃度を等しくする方向に進む。つまり、希CuSO4には銅イオンCu++ が溶け出し、銅イオン濃度を上げ、濃CuSO4から銅Cuが析出して銅イオン濃度を下げようとする。
・アノ-ド(希CuSO4) Cu → Cu++ + 2e-
・カソード(濃CuSO4) Cu++ → Cu - 2e-
|
|
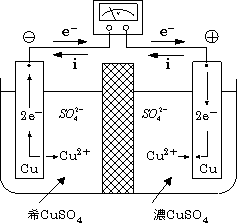
図5.3 濃淡電池
|
| (c) |
濃淡電池(通気差電池あるいは酸素濃淡電池) |
|
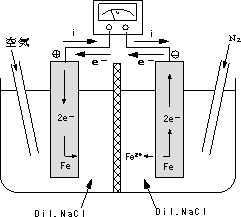
溶液中に溶解している酸素の濃度差によって電池が形成されるもので,実際の腐食環境では重要である。2個の鉄電極を希薄な食塩水に浸し,一方の電極のまわりの溶液は空気を飽和させ,他極のまわりの溶液は窒素ガスを送って溶液中の空気を追い出す。酸素の濃度差によって両極に電位差が生じ,2極を短絡すると空気を飽和した極がカソード,空気を含まない極がアノードとなって鉄が溶け出す |
|
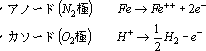 |
|
| |
図5.4 酸素の濃度差 |
|
|
次に,通気差電池によって実際に生ずる著しい損傷(すきま腐食)の例について述べる。
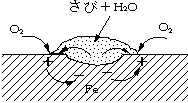
図5.5はさびやその他の反応生成物におおわれた金属面に達する酸素の量が,裸の金属面の酸素量より少なく,孔食の部分がアノード(-)となりFeが溶け出し,腐食は一層進む。その他,2本の鉄管の継ぎ目や鉄管のねじ込み部の腐食などである。
|
|
 |
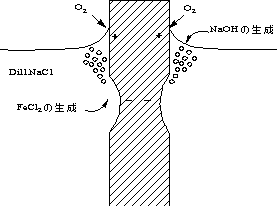 |
図5.5 鉄の腐食形態
|
図5.6 船のきっ水線が腐食される例 |
|
| (d) |
温度差電池
異なった湿度に保たれた同一組成の二つの金属電極を同一編成の電解質に浸すとこれらの電極間に電池が形成される。 |
|
|
|
| 5.3 |
腐食の分類
腐食と言うと,鉄の赤さびとか銀や銅の変色を考えるが,腐食による損傷はその他,様々な形で現われる。腐食によって割れが生じたり,金属の強度や延性が失われた結果,破損が生じる。腐食は一般的には電気化学的反応によっておこる。腐食の中には腐食生成物が肉眼ではほとんど観察できない場合や重量減少がほとんど測定出来ないほど小さい場合もある。
|
|
| (1) |
全面腐食
鉄の赤さびや銀の変色などはこの種のもので,金属の表面で均一に生ずる腐食である。金属の高温酸化(黒皮)もそうである。この全面腐食の腐食の程度は『1年間にどのくらいの量(腐食深さあるいは重量減少)の腐食をするで表す。すなわち,長期間の腐食量の平均値で表現する。
|
腐食量q mm/y |
材料の耐食性 |
|
q<0.15 |
耐食性に富む、厳しい腐食環境で使用される材料である。 |
|
0.15<q<1.5 |
比較的耐食性を許容できる。タンク配管,バルブ,ボルトの頭など |
|
q>l.5 |
実用的価値がない。 |
|
|
mm/y :全面腐食による1年間の平均板厚減少量 (mm) |
|
| (2) |
孔食, pit
孔食は局部的な腐食の形態であって,金属表面のある小さな部分の腐食速度が他の部分に比べて大きい場合である。金属表面の比較的小さな部分が固定したアノードとして働き,相当大きな速度で腐食すると深い孔食が生じ,腐食部の面積が大きい場合には浅い孔食となる。従つて,孔食の程度はしばしば最も深い孔食の深さと,試片の重量減少から換算した平均的な腐食の深さdの比,孔食係数(p/d)によって表わされる。
|
| (3) |
脱亜鉛腐食と分金
真中のような合金に生じ,合金中の亜鉛のみが選択的に腐食される。
|
| (4) |
粒界腐食
金属の結晶粒界に起こる局部的腐食で,ごく限られた面積をもつ粒界が大きい面積を持つ結晶粒と接触し,粒界がアノード,結晶がカソ-ドとなり局部電池が形成され粒界が腐食される。腐食はしばしば非常に急激に生じ,金属の内部に深く進行して,ときにはひどい破壊にいたる。18-8ステンレス鋼やアルアルミ合金(4%Cu-Al)などの腐食が代表的な例である。
|
| (5) |
応力腐食割れ,Stress Corrosion Cracking, S C C
金属が一定の引張応力の下で特定の腐食環境に置かれると一定時間後に割れを生じ破壊する。一定応力は外荷重でも冷問加工,溶接や熱処理による残留応力でも同様である。
|
| (6) |
.大気腐食
金属が大気にさらされて生ずる腐食であり,湿分が存在しなければ余り問題にならない。前述のように,腐食過程は電解質溶液がなければ進行しないからである。しかし,大気による腐食は大気に含まれる湿分ばかりでなく,金属表面への湿分の凝縮を 助ける作用をするダストの量やガス状の汚染物質濃度にも依存する。ダストは多くの大気の汚染物質として重量的に最大なもので普通の都市では大気中の量はだいたい20mg/m3程度であるが,工業地帯では1000 mg/m3 以上になる。
ダストに含まれる炭素,炭素化合物、H2SO4,(NH4)2SO4,NaClおよび他の塩類の粒子等は湿分と結びついて金属表面に電解質溶液を生成し、腐食の原因となる。大気中のガスの中で最も重要な腐食成分は,石油およびガソリンの燃焼による亜硫酸ガスSO2である。
|
| (7) |
土壌腐食
埋設されたバイプラインの腐食の現象が良い例である。大気腐食と類似し,腐食速度は土壌の種類やタイプによつて異なり,大気腐食より大きい。土壌の腐食性を決定する要因としては,通気性,電気伝導度,溶解塩,湿分,酸性アルカリ度などである。 |
|
|
|
| 5.4 |
応力腐食割れ Stress Corrosion Cracking, SCC |
|
応力腐食割れは腐食環境,材料,負荷荷重の3要素か同時に関与して生ずる現象である。従って.それぞれの要素の効果を別々に考えるのてはなくて総合的に取り扱われなければならない。破壊におよぼす影響は3要素の相乗効果となって表われる。
応力条件下においては,無負荷状態における通常の腐食を加速させるが、これは、孔食の発生により,応力集中が生じ、さらに,転位の移動によるすべりの発生,表面酸化膜の破壊,すべりにより新たに環境にさらされていない金属表面の出現等が繰り返される。これらの現象が腐食を加速させる原因になっている。
一見無負荷状態にある金属においても、加工時の塑性変形における残留応力の存在、溶接箇所の残留応力,温度変化による熱応力など応力腐食割れと考えた方がよい場合が多い。 |
|
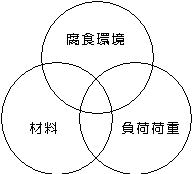
図5.7 応力腐食割れの3要素 |
|
|
| (1) |
負荷応力と破断までの時間
図5.8は腐食環境中にて切欠き付きの試験片に一定な応力を負荷して破断まての時間を求めたものてある。3%食塩水の腐食環境中における場合についてみると,応力が大きいと破断まての時間は短く,逆に小さい場合は長くなっている。応力腐食割れに及ぼす影響(SCC感受性)は3%食塩水の場合が顕著である。また,このように,時間に依存する破壊を『遅れ破壊(Delayed fracture)』ともいう。 |
|
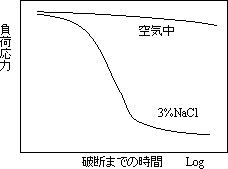
図5.8 一定負荷の大きさと破断までの時間の関係
|
| (2) |
応力腐食割れの機構 |
|
| ① |
機械的破壊作用が主役 |
|
腐食によるピットの切欠き効果,粒界,析出相などの障害による転位の集積による局所的応力集中によって塑性変形し、すべりが生じ,酸化被膜等を破壊し,新生面が形成され,この部分の腐食が更に進行する。その後,この過程を繰り返しき裂が成長する。腐食環境中のH2,その他のものが欠陥や割れ目に吸着して材料の表面エネルギーγが低下し,グリフィスの破壊条件式(長さ2cのき裂が存在するとき,応力がσfに達したとき、き裂は進展を開始し、破壊が始まる)
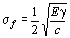
E:ヤング係数,γ:表面エネルギー, c:き裂長さの半分
の破壊応力σfを下げる。これが核となってき裂が成長する。
|
| ② |
活性点(アノード)の生成 |
|
一般に純金属は応力腐食割れは生しない。応力を与えなくとも合金中の不純物の偏析,析出物の存在のために粒界が結晶粒に対してアノードになり易い。そして,応力を与えたときは,転位の増殖によってすべりが生し,常温においても拡散が盛んとなってN,Cなどの格子間原子は容易に拡散して欠陥部に偏析する。こうして出来た成分偏析はアノードまたはカソードとして働き得る。 |
|
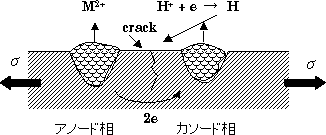
(a) 不純物の偏析 局部電池の形成 |
|
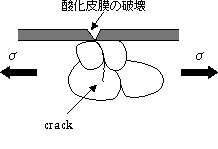
(b) 酸化皮膜の破壊、炭素鋼の黒皮は腐食に対して抵抗となっている |
|
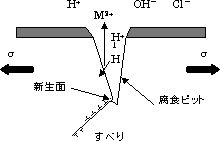
(c)酸化皮膜の破壊の後、腐食によるピットの生成、応力集中によるすべりの発生、
新生面ができ、これがまた腐食する。
水素原子は小さいため、金属に侵入,原子間結合力,表面エネルギーを弱める。
|
|
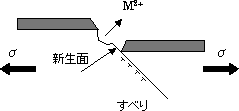
(d) すべりによる酸化皮膜の破壊、新生面の出現、腐食進行
図5.9 応力下での腐食の機構
|
|
 |
 |
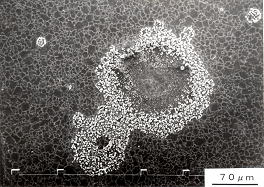
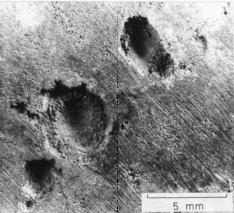
| (a) |
(b)ピットの断面形状 |
|
|
図5.10 石油タンク底板の腐食ピット、SS400
|
|
石油タンク破損事故は底板と側板のT型溶接部の近傍が多い。この部分は、タンク稼働時に最も大きな応力が作用する箇所であり、溶接時の残留応力も存在する。容量一万トンクラスのタンクで溶接部の側板19mmで、アニュラー板(T型溶接部の底板)8mm、底板6mmで材質はSS400である。腐食はアニュラー板裏側(地面側)で生じ、応力の存在と雨水の侵入などが腐食を発生させる原因の一つとされている。現在は、大型石油タンクの場合、10年に1回の板厚保測定が行われ、腐食よる減肉量が定められた量に達した箇所の板材交換の処理を行っている。腐食は確率現象であるので、私たちは、板厚測定データから、確率統計的に残存寿命を推定する方法を提案している。
極値統計法による腐食材の残存寿命推定
|
|
| 5.5 |
水素ぜい性,遅れ破壊 |
|
応力を負荷したとき水素のような小さな侵入型の元素は電解質溶液から金属に容易に移動する。その結果,金属の結合力や表面エネルギーが低下する。遅れ破壊時間はき裂先端の応力集中領域への水素の拡散,偏析するまての時間として説明されている。
|
| 5.6 |
腐食疲労 |
|
金属が腐食性の環境で繰り返し荷重を受けると疲労現象が一層促進される。これを腐食疲労と言う。環境が腐食環境でない場合,鋼は一般に耐久限度(この大きさの応力振幅以下の荷重に対しては金属は無限の練り返しに耐える)を示すが,環境が腐食性の場合は耐久限度を示さなくなる。つまり小さな応力でも繰り返し負荷ざれると腐食性環境では疲労破壊することを意味している。 |
|
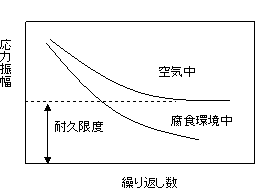
図5.11 鋼材のS-N曲線で、腐食環境中では耐久限が消失する
|
| 5.7 |
腐食の実例 |
|
| ■ |
腐食疲労
図5.12は漁網取り付け金具が、海水中で疲労破壊を起こした破面である。表面近くで偏析した不純物が破壊の基点になっており、ストライエーションの形状も空気中のものとは様相が異なっている。
|
|
 |
 |
(a)海水中での炭素鋼の腐食疲労
疲労き裂発生部近傍 |
(b ) 腐食疲労破面の拡大写真 |
図5.12 炭素鋼の海水中における疲労破壊
|
| ■ |
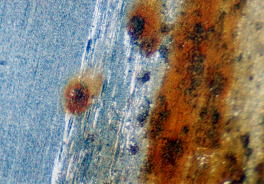
ステンレスのすき間腐食 |
|
ステンレスの場合,炭素鋼と異なり,一般的には腐食は受けないのが通例である。しかし、異物が載った場合は場合はすきま腐食を生ずる(図5.13(a))。図5.13(b)は、SUS304ステンレス板の上に炭素鋼の鉄粉を載せ水道水に浸した場合で、白い部分は鉄粉の腐食時の酸化物であるが中心部ではステンレスに腐食ピットが生じていた。 |
|
図5.13 ステンレスのすき間腐食
|
| ■ |
Eガラス(FRPの強化繊維)の腐食 金属以外の腐食例 |
|
図5.14は無負荷でのEガラス繊維の腐食の様相を示したもので、,3.5%HCl水溶液環境中である。ガラス中のCaとAlが酸中にイオンとなって溶け出し,分子容の変化が生じた結果,表面層と酸に犯されていない繊維中心部間に応力分布が発生し,酸による応力腐食割れによりき裂が生ずると報告されている.しかしながら,腐食の形態から,繊維製造時の残留応力の分布状態も大きく影響していると推定される.荷重を負荷した場合は一層腐食が進む結果を得ている。 |
|

図5.14 無負荷でのガラス繊維の腐食の様相,3.5%HCl水溶液環境
|
| ■ |
3.5%HCl水溶液環境中での複合材の疲労試験 |
|
プラントの複合材が酸によって腐食を受けることが問題になっている。図5.14に示したようにEガラス繊維が腐食を受け,強化材の役割を果たさなくなるのが主たる原因であるが,図5.15はポリカーボネイトに1%のガラス繊維を含む材料の疲労試験において表面から発生したき裂の近傍の写真である。き裂先端の領域にはポリカーボネイトに編目状のき裂が発生していた。空気中の疲労試験では見られなかった現象で,応力の下ではポリカーボネイトも酸により何らかの影響を受けることが判明した。 |
|
|
 |
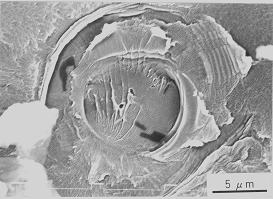 |
| 図5.15疲労き裂先端領域の網目状の表面き裂 ,3.5%HCl水溶液環境、PC材 |
図5.16 疲労破面の様相,
3.5%HCl水溶液環境、PC材 |
|
|
図5.16は3.5%HCl水溶液環境中の疲労破面の様相であるが,強化材であるガラス繊維は疲労き裂に対して余り抵抗となっていないことを示している。 |
|
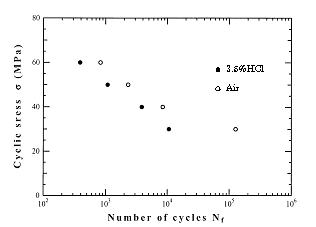
図5.17 3.5%HCl水溶液中におけるAS材のS-N曲線
|
|
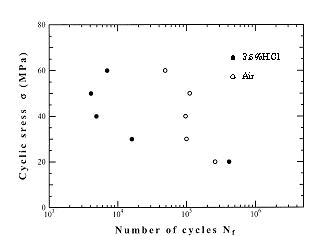
図5.18 3.5%HCl水溶液中におけるPC材のS-N曲線
|
|
腐食の問題は、学際的な問題であり、材料、腐食環境、荷重の組み合わせが多種であり、パラメータが多く、実用的には厄介な問題である。特に、環境と材料の組み合わせごとに、腐食の様相が異なる。
|
|
種々の金属に対する腐食環境を表に示した。
|
|
表 金属と腐食環境1)
|
|
|
|
参考文献
|
|
1) 金属の腐食損傷と防食技術,小若正倫,アグネ(1983). |
|
2)「腐食反応とその制御」,ユーリック著,岡本他訳,産業図書
* 腐食について書かれている最も権威のある著書である |
|
|