| 3.相律と二元系状態図 |
||||||||||||
| 3.1 相,成分及び相律 |
||||||||||||
| a.相(phase) 物質の“すがた” , 気相,液層,固相 「1つの系において他の部分と明らかに境界を持って区切られ,それ自身の中では均質である部分」 ・水と油の混合 二層に分かれる,境界は明らか 異なった液相共存 ・合金の場合は,結晶構造の異なる固相が存在しうる b.成分 Component 1つの系を構成するもとになる物質 すべての元素,化合物 (1).それらの量を適当に変えることによって,その系のいずれの相の組成を表しうる (2).1つの成分の量の変化は,他の成分の量とは独立に存在しうる Ex.1 食塩水の場合 水(H2O)と食塩(NaCl)の量は自由に変えられる。 独立成分 H,O,Na,Clは勝手に変えられない Ex.2 合金(炭素鋼 FeとCの合金)の場合 ・元素そのものが独立成分 ・ FeとCの化合物も独立成分 |
||||||||||||
| C.相律 phase rule ・平衡 equilibrium 熱的な釣り合い、合金系に外から熱を加えず、また奪わない(断熱状態)で長く放置したときに似た状態 ・相の数 r 個, ・自由に決められる変数は・・・・ 温度,圧力,各相の組成 ・自由度f (freedom) 平衡関係を変えずに自由に変えうる変数の数 f = n+2-r 合金の平衡状態を律する法則,熱力学の理論 ・f = 1を1変系,f = 2 を2変系, ・f = 0を不変系 一定温度,一定圧力下で相変化する ・圧力の影響は大気中では小さい, 変数が一つ減る f=n+2-r-1 → f=n+1-r 凝縮系の相律 |
||||||||||||
| 3.2 状態図の構成 |
||||||||||||
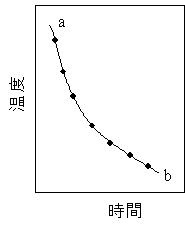
| ・熱分析 状態図を求める基本的な方法 物質を高温から冷却しながら,一定時間毎に物質の温度を計測,その結果を横軸に時間縦軸に温度をとり関係曲線をグラフで表す ・合金の変態点では曲線に変化が表われる.変化がなければ曲線は滑らか |
||||||||||||
図1 温度の時間的変化 |
||||||||||||
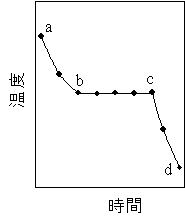
| 温度の時間的変化のグラフ(図1) ・配列状態の変化により,潜熱が発生,温度降下が遅れる ・純金属の場合の相律の適用 液相から固相に変態するとき、 成分数 n =1, 相の数r=2(液相,固相) ∴ f = n + 1 - r = 1+ 1-2 = 0 自由度=0 温度一定 b-c間の現象 ・加熱の場合は逆の現象 |
||||||||||||
|
||||||||||||
|
||||||||||||
| |
||||||||||||
| 3.4 基本状態図Ⅰ ■ H2O - NH4Clの場合(塩化アンモニュウム水溶液の冷却) 金属の状態図を調べる前に、塩化アンモニュウム水溶液の冷却の場合の相変化を調べてみる。 |
||||||||||||
| ●9.1%NH4Cl水溶液(a)の場合 -6.6℃ 水溶液温度-6.6℃ 水溶液に濁りが生ずる→水の結晶:氷 |
||||||||||||
| NH4Cl水溶液 → 純粋な水の結晶:氷 ---- 初晶 氷の量が大になるにつれ水溶液のNH4Cl濃度上昇,変態温度は下降 |
||||||||||||
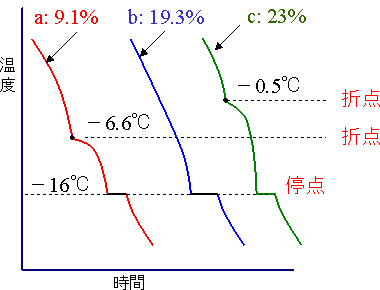 図1 塩化アンモニュウム水溶液の冷却 |
||||||||||||
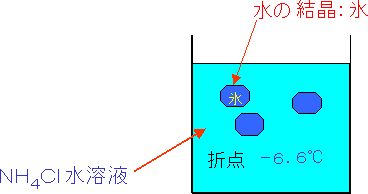 図2 水溶液温度-6.6℃ |
||||||||||||
| ●9.1%NH4Cl水溶液(a)の場合 -16℃ ・水溶液温度-16℃では水溶液濃度19.3%、 ・NH4Cl水溶液 → 共晶の氷+NH4Clの結晶が同時に晶出 ・共晶 水溶液が完全に変態完了するまで温度一定,-16℃ ・変態完了後温度降下,変態完了後の相 純粋な氷(初晶+共晶の氷) +NH4Clの結晶 初晶:-6.6℃で生成した結晶 |
||||||||||||
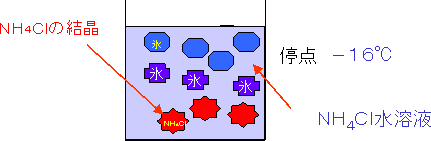 図3 9.1%NH4Cl水溶液温度-16℃ |
||||||||||||
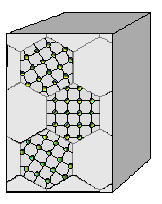
9.1%NH4Cl水溶液の固相組織
|
||||||||||||
| ●19.3%NH4Cl水溶液(b)の場合 -16℃ 水溶液温度-16℃, NH4Cl水溶液→ 氷 + NH4Clの結晶 2つの結晶が同時に晶出 共晶反応 |
||||||||||||
 図4 19.3%NH4Cl水溶液温度、-16℃ |
||||||||||||
19.3%NH4Cl水溶液の固相組織
|
||||||||||||
| ●23%NH4Cl水溶液の場合(c) 水溶液温度-0.5℃ ・水溶液温度-0.5℃ NH4Clの結晶 NH4Cl水溶液→NH4Clの結晶 初晶 NH4Clの結晶の量が大になるにつれ<<水溶液の濃度低下,変態温度は下降 |
||||||||||||
 図5 23%NH4Cl水溶液温度-0.5℃ |
||||||||||||
| ●23%NH4Cl水溶液の場合(c) 水溶液温度-16℃,水溶液濃度19.3% NH4Cl水溶液 → 氷+NH4Clの結晶が同時に晶出 共晶,水溶液が完全に変態完了するまで温度一定,-16℃ ・変態完了 温度降下 純粋な氷+NH4Clの結晶(初晶+共晶) |
||||||||||||
 図6 23%NH4Cl水溶液温度-16℃ |
||||||||||||
23%NH4Cl水溶液の固相組織
|
||||||||||||
| ■単一共晶系状態図 | ||||||||||||
| 図7のように、横軸に濃度、縦軸に温度をとり、いろいろな濃度で、折点、停点を求め温度と濃度の関係曲線を求めると状態図が得られ、各領域における組織が判明する。 金属の場合も同様に状態図を求めることができる。 |
||||||||||||
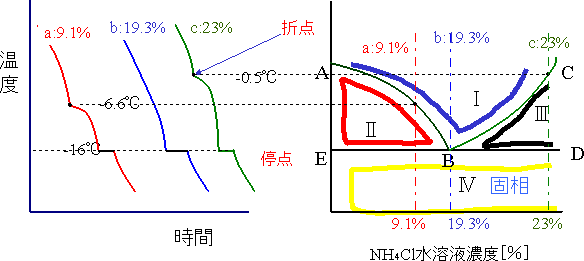 図7 単一共晶系状態図 |
||||||||||||
|
||||||||||||
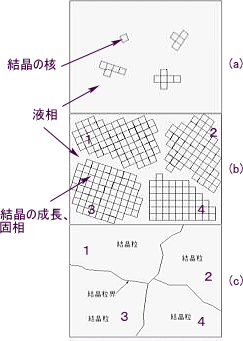
| ■固相 界域Ⅳの詳細 |
||||||||||||
界域Ⅳの詳細
|
||||||||||||
| AB,BC:初晶線、 B : 共晶点 BD : 共晶を生ずる温度 |
||||||||||||
| *共晶反応 均一溶液 → 純粋な結晶A +純粋な結晶B | ||||||||||||